Добавление обращения о нежелательных реакциях
Предназначение операции
Операция предназначена для регистрации информации о нежелательной реакции при применении лекарственного средства.
Предусловия и подготовительные действия
Для реализации функции средствами системы необходимо выполнить следующие действия:
- Открыть компонент «Гален».
- Открыть раздел «Обращения о нежелательных реакциях».
Основные действия
Для осуществления работы с обращениями о нежелательных реакциях могут быть выполнены следующие действия:
Добавление нового обращения
Для добавления нового обращения необходимо выполнить следующие шаги.
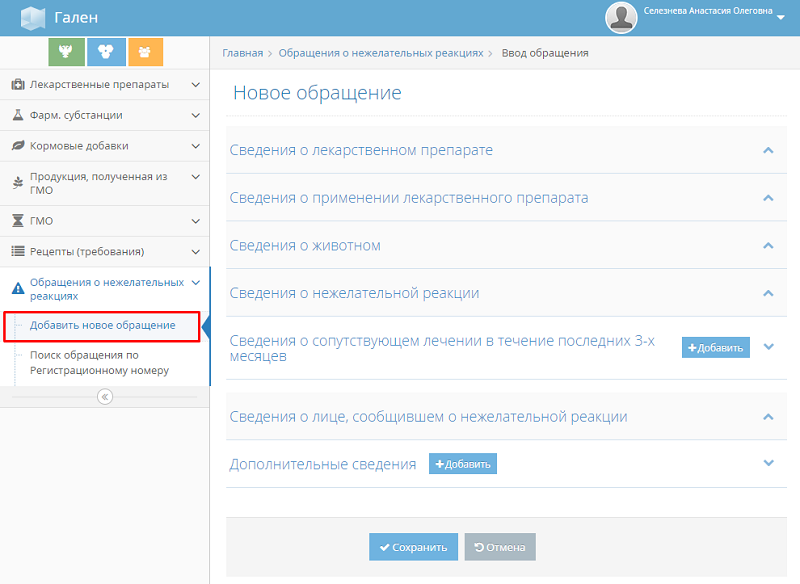
- В выпадающем списке выберите подраздел «Добавить новое обращение». В результате откроется страница «Новое обращение».
- На открывшейся странице добавления нового обращения внесите сведения о лекарственном препарате и о его применении, сведения о животном, о нежелательной реакции, о сопутствующем лечении, а также укажите информацию о заявителе (рис. 1).
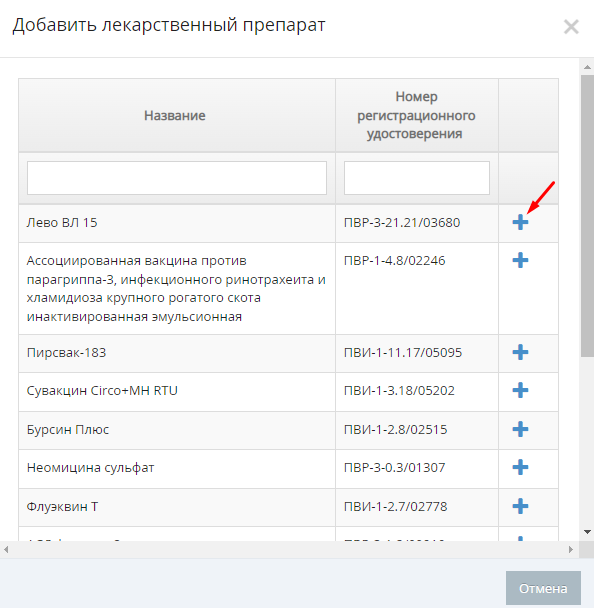
Обратите внимание, пиктограммой * выделены поля, обязательные к заполнению, а заполненные блоки информации для удобства возможно свернуть, нажав на название блока. - В блоке «Сведения о лекарственном препарате» выберите лекарственное средство. Для этого нажмите на кнопку «Добавить из списка» (пиктограмм «плюс»). В результате откроется модальное окно «Добавить лекарственный препарат» (рис. 2).
- 3.1. В открывшемся модальном окне отображается весь список Реестра лекарственных препаратов (далее – ЛП). Осуществите поиск ЛП по названию или по номеру регистрационного удостоверения.
- 3.2. После осуществления поиска нужного ЛП нажмите на кнопку «Выбрать» (пиктограмм «плюс») для добавления препарата. В результате модальное окно добавления лекарственного препарата будет закрыто.
- 3.3. Заполните следующие сведения о препарате:
- наименование производителя (доступен только выбор значения из выпадающего списка);
- номер серии;
- дата производства;
- срок годности;
- доза;
- путь введения;
- * дата начала применения;
- дата окончания применения;
- показания.
- В блоке «Сведения о применении лекарственного препарата» заполните следующие поля:
- условия применения лекарственного препарата для ветеринарного применения (амбулаторное/стационарное/по назначению специалиста в области ветеринарии/самостоятельно, без назначения специалиста в области ветеринарии);
- * количество животных, которым вводился лекарственный препарат;
- * количество животных, у которых возникли нежелательные реакции;
- * сопровождалась ли отмена лекарственного препарата исчезновением нежелательной реакции? (да/нет/лекарственный препарат не отменялся);
- * назначался ли лекарственный препарат повторно? (да/нет);
- если в предыдущем поле выбрано значение «да», укажите результаты повторного назначения.
- В блоке «Сведения о животном» заполните следующие поля:
- * вид (доступен только выбор значения из выпадающего списка);
- порода;
- пол (самец/самка/смешанный);
- вес;
- возрастная группа;
- * аллергия (есть/нет/неизвестно);
- * стерилизовано (есть/нет/неизвестно).
- В блоке «Сведения о нежелательной реакции» заполните следующие поля:
- * вид нежелательной реакции (побочное действие/нежелательная реакция/серьезная нежелательная реакция/непредвиденная нежелательная реакция);
- * описание;
- в том числе данные лабораторных исследований;
- дата начала нежелательной реакции;
- * клиническое состояние животного(ых) после применения лекарственного препарата (смерть/угроза жизни/угроза здоровью);
- предпринятые меры (без лечения/отмена лекарственного препарата/снижение дозы лекарственного препарата/немедикаментозная терапия/лекарственная терапия);
- если в предыдущем поле выбрано значение «лекарственная терапия», укажите информацию о лекарственной терапии в появившемся поле «Лекарственная терапия».
- * исход нежелательной реакции (выздоровление без последствий/улучшение состояния/состояние без изменений/смерть/выздоровление с последствиями/исход не известен на дату направления сообщения);
- дата окончания нежелательной реакции.
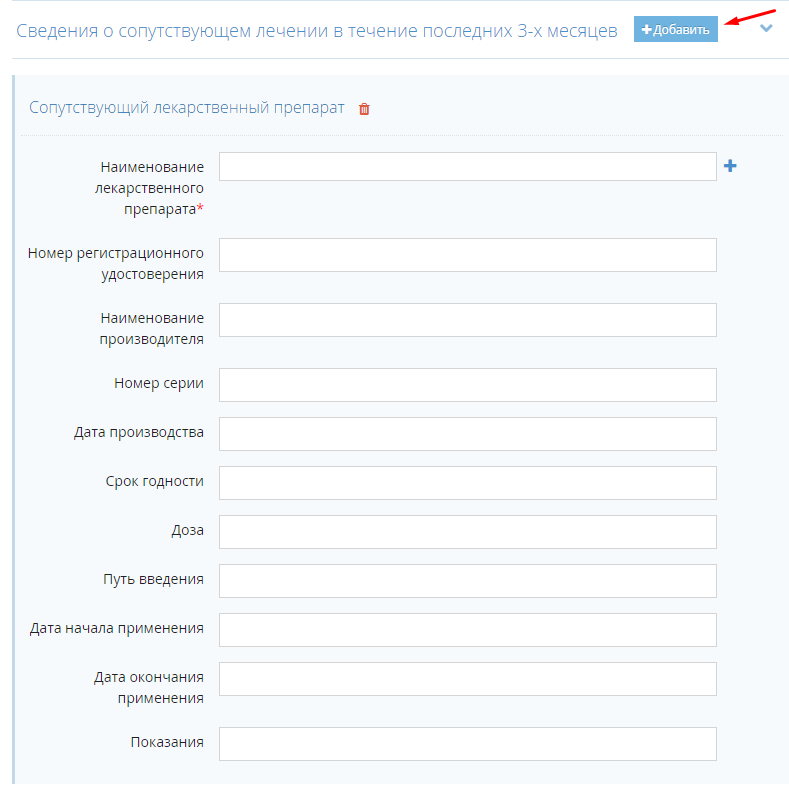
- Для добавления информации о сопутствующем лечении в течение последних 3-х лет нажмите на кнопку «Добавить» (рис. 3). В результате на форме ввода данных отобразится новый блок для введения значений «Сопутствующий лекарственный препарат».
- 7.1. В блоке «Сопутствующий лекарственный препарат» заполните следующие поля:
- * наименование лекарственного препарата, схема добавления идентична п. 3;
- после добавления наименования номер регистрационного удостоверения заполнится автоматически из справочника;
- наименование производителя (доступен только выбор значения из выпадающего списка);
- номер серии;
- дата производства;
- срок годности;
- доза;
- путь введения;
- дата начала применения;
- дата окончания применения;
- показания.
- 7.2. Для удаления дополнительной формы ввода данных нажмите на кнопку «Отменить добавление» (пиктограмм «корзина»).
- 7.3. Для добавления информации об еще одном сопутствующем лечении в течение последних 3-х лет повторите действия, начиная с п. 7.
- 7.1. В блоке «Сопутствующий лекарственный препарат» заполните следующие поля:
- В блоке «Сведения о лице, сообщившем о нежелательной реакции» заполните следующие поля:
- * заявитель (специалист в области ветеринарии/владелец животного/иной субъект обращения лекарственных средств);
- * тип заявителя (юридическое лицо/физическое лицо);
- * ФИО или полное наименование юридического лица;
- * ИНН;
- * КПП;
- * ОГРН;
- * регион (доступен только выбор значения из выпадающего списка);
- населенный пункт (доступен только выбор значения из выпадающего списка);
- * адрес;
- * адрес электронной почты;
- контактный телефон;
- * признак получения обращения (заполнено автоматически).
- При необходимости укажите дополнительные сведения. Для этого в блоке «Дополнительные сведения» нажмите на кнопку «Добавить». В результате откроется блок добавления файлов.
- 8.1. В открывшемся блоке выберите или перетащите файл, при необходимости оставьте комментарий.
- 8.2. Для удаления дополнительной информации нажмите на кнопку «Отменить добавление» (пиктограмм «корзина»).
- В блоке «Согласие на обработку персональных данных» подтвердите согласие, нажав на чек-бокс «Согласен на обработку персональных данных». При необходимости ознакомьтесь с Политикой конфиденциальности.
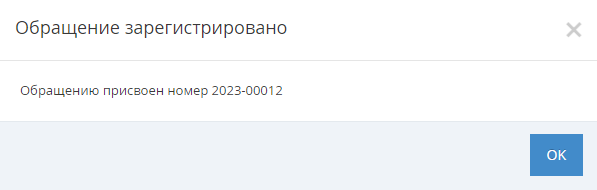
- Для отправки обращения на рассмотрение нажмите на кнопку «Сохранить». В результате заявке автоматически будет присвоен регистрационный номер (рис. 4).
Вернуться к основным действиям ↑
Заключительные действия
В результате выполненных действий будет зафиксировано обращение Заявителя о нежелательной реакции при применении лекарственного препарата. Вернуться к началу ↑
Исключительные ситуации
По техническим вопросам, связанным с работой компонента «Гален», обращаться по электронной почте на адрес galen@fsvps.ru.
Ресурсы
Временные затраты на регистрацию обращения составляют не более двух минут.
Ссылки
- https://galen.vetrf.ru/— Веб-интерфейс компонента «Гален».